| Los trastornos respiratorios durante el sueño incluyen el ronquido, síndrome de apnea/hipopnea del sueño (obstructiva, central o mixta), el insomnio, hipersomnias (narcolepsia), parasomnias (pesadillas), síndrome de piernas inquietas, etc. Estos trastornos aparecen en todas las edades (niños, adolescentes, adultos). - PRIMER AUTOR
Marcos Moradas Estrada. DDs
Profesor asociado. Servicio de Odontología Conservadora de la Clínica Universitaria de la Universidad de Oviedo
- Servicio de Odontología Conservadora y Materiales Odontológico. Dpto de Cirugía y Especialidades Médico Quirúrgicas de la Universidad de Oviedo Beatriz Álvarez López
Licenciado en Odontología. Dentista área sanitaria nº I Servicio de Salud del Principado de Asturias. Práctica privada en Tapia de Casariego. - Email autor responsable: marcosmords@gmail.com
c/ Catedrático Serrano s/n - Clínica Universitaria de Odontología, 3º planta. Despacho Prfs Asociados 2. Oviedo - ASTURIAS
RESUMEN
La utilización de aparatos intraorales para tratar la obstrucción de la vía aérea superior no es un concepto nuevo, pues ya en 1934, Pierre Robin aconsejaba la utilización de su monoblock con el objeto de realizar un desplazamiento funcional de la mandíbula hacia una posición más adelantada, aumentando así el tamaño de la vía aérea superior y evitando la glosoptosis en los niños que presentaban micrognatismo mandibular severo.
La Asociación Americana de Alteraciones del Sueño (ASDA), define los aparatos intraorales destinados a tratar el SAHOS como: «dispositivos que se introducen en la boca para modificar la posición de la mandíbula, lengua y otras estructuras de soporte de la vía aérea superior para el tratamiento del ronquido y/o la apnea obstructiva del sueño». La utilización de los aparatos intraorales en este tipo de patología surgió en la década de los 80 en un intento de encontrar métodos alternativos tanto a la cirugía (UPPP, ortognática, etc.) como a la nCPAP2*. Los aparatos intraorales en el tratamiento del SAHOS ofrecen grandes ventajas en algunos enfermos. Son cómodos y fáciles de manejar por el paciente, no son invasivos, de acción reversible, baratos, fáciles de fabricar y generalmente bien aceptados por el paciente ABSTRACT The use of intraoral devices to treat upper airway obstruction is not a new concept, since as early as 1934 Pierre Robin advised the use of his monoblock in order to perform a functional displacement of the mandible towards a more advanced position, Thus increasing the size of the upper airway and avoiding glossoptosis in children with severe mandibular micrognathism. The American Sleep Disorders Association (ASDA) defines intraoral appliances intended to treat OSAHS as: 'devices that are inserted into the mouth to modify the position of the mandible, tongue, and other upper airway support structures to The treatment of snoring and / or obstructive sleep apnea. The use of intraoral devices in this type of pathology arose in the 1980s in an attempt to find alternative methods to both surgery (UPPP, orthognathic, etc.) and nCPAP2 *. Intraoral devices in the treatment of OSAHS offer great advantages in some patients. They are comfortable and easy to handle by the patient, non-invasive, reversible, cheap, easy to manufacture and generally well accepted by the patient
MATERIAL y METODO
Se ha realizado una revisión bibliográfica descriptiva de las evidencias aportadas en artículos indexados y otras fuentes bibliográficas, como libros, tesis u otros. Se obtuvo un total de 225 resultados. Éstos se analizaron y tras comprobar si cumplían o no los criterios de inclusión/ exclusión de éste trabajo, finalmente fueron 43 los artículos de revisión bibliográfica publicados en un horquilla que va de 2010 a 2014, habiendo 5 artículos de 1994 y 1996, en lo referente a datos históricos, con los que ayudar a plantear el estado actual de la cuestión. KEY WORDS: apnea, hipoapnea, via aérea, sleep troubles, bruxism, oral treatment,
1. INTRODUCCIÓN
El síndrome de la apnea o hipopnea del sueño se caracteriza por una serie de problemas como: somnolencia excesiva diurna, respiratorios, cardiacos, metabólicos o inflamatorios debido a episodios repetidos de obstrucción de la vía aérea superior durante el sueño. La persona que lo padece se despierta repetidamente con la consecuencia de un sueño no reparador. Según la Sociedad Española de Patología Respiratoria lo define de la siguiente manera:
"cuadro de somnolencia, trastornos neuropsiquiátricos, respiratorios y cardiacos secundarios a episodios repetidos de obstrucción de la vía aérea superior que provocan repetidas desaturaciones de la oxihemoglobina y despertares transitorios que dan lugar a un sueño no reparador" y la Academia Americana de Sueño (AASM) lo delimita en tres apartados:
• Un Índice de Alteración Respiratoria mayor o igual a 5 (IAR ≥ 5) incluyendo la presencia de esfuerzos respiratorios asociados a microdespertares.
• Excesiva somnolencia diurna.
• Dos o más de los siguientes:
- Asfixias durante el sueño.
- Despertares recurrentes.
- Torpeza al despertar.
- Fatiga durante el día.
- Dificultades de concentración.
Debido a que puede ser central, mixta u obstructiva he elegido el Documento de Consenso Nacional sobre el Síndrome de Apneas-Hipopneas durante el Sueño (SAHS) del Grupo Español de Sueño donde han clasificado las siguientes definiciones sobre los principales eventos respiratorios de la siguiente manera:
TIPO DEFINICIÓN SEGÚN SAHS
Apnea obstructiva Ausencia o reducción > 90% de la señal respiratoria (termistores, cánula nasal o neumotacógrafo) de > 10 segundos de duración en presencia de esfuerzo respiratorio detectado por las bandas toraco-abdominales.
Apnea central Ausencia o reducción > 90% de la señal respiratoria (termistores, cánula nasal o neumotacógrafo) de > 10 segundos de duración en ausencia de esfuerzo respiratorio detectado por las bandas toraco-abdominales.
Apnea mixta Es un evento respiratorio que, habitualmente, comienza con un componente central y termina en un componente obstructivo.
Hipopnea Reducción discernible (> 30% y < 90%) de la amplitud de la señal respiratoria de > 10 segundos de duración (termistores, cánula nasal o neumotacógrafo) que se acompaña de unas desaturación (> 3%) y/o un microdespertar en el EEG.
Esfuerzos
Respiratorios
Asociados a microdespertares
(ERAM) Período > 10 segundos de incremento progresivo del esfuerzo respiratorio (habitualmente detectado mediante medición de presión esofágica) que acaba, con un microdespertar. Opcionalmente, también pude detectarse el esfuerzo mediante el empleo de una cánula nasal y/o el sumatorio de las bandas toraco-abdominales cuando hay un período de limitación al flujo > 10 segundos y < de 2 minutos, sin reducción marcada de la amplitud del flujo y que termina con un microdespertar
2. FISIOPATOLOGÍA
Respecto a lo anatómico, la vía aérea superior (VAS) es un tubo músculomembranoso y está formado por tres estructuras: las fosas nasales, la faringe y la laringe. A su vez, la faringe la podemos dividir en: rinofaringe o nasofaringe, orofaringe e hipofaringe o laringofaringe. Para que se produzcan los movimientos respiratorios necesitamos la participación activa de dos grupos musculares: músculos que generan presión como puede ser el diafragma y los músculos de la VAS donde encontramos suprahioideos, infrahioideos, elevadores y constrictores de la faringe. Cuando todo funciona correctamente existe un equilibrio entre la fuerza de los músculos inspiratorios y los músculos dilatadores faríngeos, permitiendo el intercambio gaseoso adecuado y la permeabilidad de la vía aérea superior. A veces durante el sueño, se producen cambios en la respiración ya que es menos riguroso el control respiratorio en comparación con la vigilia. En cambio, cuando este patrón respiratorio se altera, podemos padecer un trastorno respiratorio del sueño. Pueden aparecer trastornos no obstructivos u obstructivos. Éstos, los cuales serán en los que nos centremos en este trabajo, tienen como rasgo primordial el colapso de la faringe, así como la presencia del ronquido. Por eso, al síndrome de la apnea-hipopnea obstructiva del sueño tiene una triada típica que se caracteriza por: ronquido, paradas respiratorias y somnolencia diurna.
Pero actualmente, la fisiopatología no está muy clara y no se conoce muy bien. Pero estos esquemas muestran los mecanismos fisiopatológicos y sus consecuencias de una forma bastante resumida. En los siguientes esquemas podemos ver que quien padece este trastorno puede llevarle incluso a la muerte súbita, por eso es muy importante diagnosticarla y poner los medios disponibles para un buen tratamiento para quien la sufre. 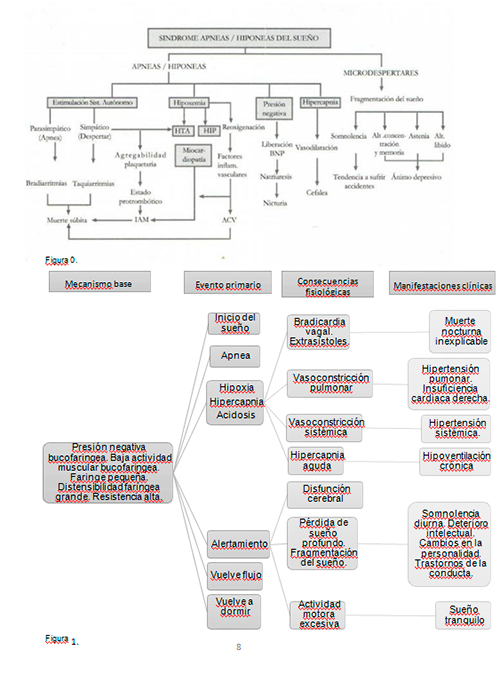
También, aparte de la fisiopatología, tenemos que tener en cuenta los factores que favorecen el colapso de la VAS ya que presentará una probabilidad mayor de poder padecer el trastorno y así aparecer las manifestaciones clínicas y consecuencias fisiológicas anteriormente esquematizadas. Los factores son los siguientes:
- Edad ya que a medida que degeneramos perdemos tono muscular y puede aumentar la probabilidad de padecerlo.
- El sexo, en los hombres es mucho más común que en las mujeres ya que los estrógenos protegen los músculos del cuello. Aunque hay que tener en cuenta que después de la menopausia puede ampliar la probabilidad.
- Obesidad o sobrepeso porque se cierra la luz de la VAS debido a la flacidez de los musculos del cuello por exceso de peso.
- Tabaco y alcohol ya que irritan estructuras como la úvula o faringe.
- Factores anatómicos como la desviación del tabique nasal, la úvula de tamaño mayor, estructuras orales las cuales hablaremos más adelante cuando profundicemos en el papel del odontólogo en la exploración.
- Factores patológicos, pólipos o tumores en la VAS, tejidos inflamados e hipertrofiados. Enfermedades o miopatias que generan un deficiente control motor del tono muscular en las estructuras del cuello.
3. SÍNTOMAS Y SIGNOS
Después de tener claro las dos manifestaciones más importantes como la apnea y los microdespertares, catalogamos a la enfermedad con la triada anteriormente dicha:
- Roncopatia, ronquidos ruidosos.
- Apneas, caracterizadas por paradas respiratorias.
- Somnolencia excesiva diurna.
Por todo esto, debemos recordar que a la consulta de un odontólogo puede ir alguien que aún no ha sido diagnosticado del SAHS por lo cual es importante tener claro los síntomas y signos que nos podemos encontrar en clínica.
Primeramente, es fundamental incluir en la historia clínica odontólogica preguntas como:
- ¿Tiene paradas respiratorias durante el sueño?
- ¿Se queda dormido durante el día?
- ¿Ronca mientras duerme?
- En el apartado de enfermedades, ¿tiene algún trastorno del sueño?
Ya que en las actuales historias habitualmente no viene.
SÍNTOMAS
El paciente se puede quejar de que no duerme lo suficiente, tiene dificultades para concentrarse, presenta reflujo gastroesofágico, cefalea matutina, mal aliento u otros síntomas no identificables por los odontólogos como disminución de la líbido, pesadillas, sueño agitado...
SIGNOS
Nuestro examen queda limitada a la exploración de cabeza y cuello y hay muchos signos que podemos observar y pueden ser factores de riesgo asociados al SAHS.
- En el interior de la cavidad oral podemos encontrar a la lengua la cual puede aumentar la probabilidad de obstruir la VAS ya que puede tener
un tamaño más de lo normal. Como la macroglosía. También fisuras o lengua saburral por su relación con el reflujo gastroesofágico. Una lengua saburral es una lengua blanquecina, también puede estar relacionada con otras enfermedades o mala higiene oral.
- Presencia de boca seca.
- Úvula hipertrofiada, inflamada. Acentúa el ronquido o el SAHS.
- Basándonos en los grados de Mallampati realizados con la boca abierta al máximo, en posición sentada y sin fonación exploraremos la orofaringe, úvula y paladar blando. Cuanto más aumenta el grado, peor es el acceso a la VAS, es decir hay más obstrucción y por lo tanto aumenta la probabilidad de padecer SAHS. 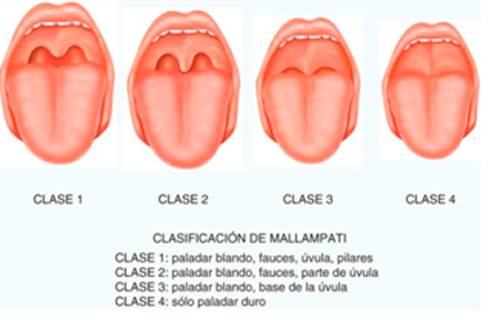 Figura 2.
- Paladar duro, observar si es estrecho y profundo.
- Podemos reconocer si es un respirador bucal o no fijándonos en el sellado labial, viendo si es tenso, forzado... La mejor pauta es que los labios estén juntos sin tensión.
- Observar el estado periodontal. También podremos ver si hay erosión en los dientes, erosión, abfracción...ya que podemos estar ante un posible paciente que padece bruxismo del sueño.
- El tamaño de las amígdalas también pueden favorecer a la obstrucción de la VAS: 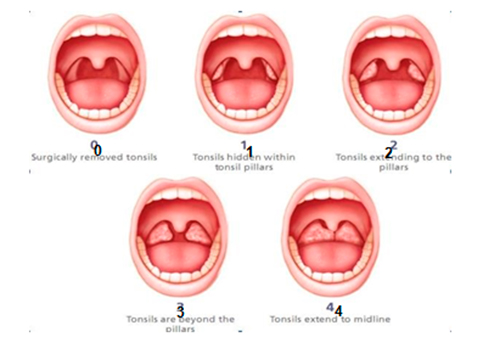 • Grado 0: Amígdalas no visibles.
• Grado 1: Amígdalas palatinas visibles, sin sobrepasar pilares.
• Grado 2: Amígdalas que sobrepasan los límites de los pilares.
• Grado 3: Amígdalas que sobrepasan los límites de los pilares y alcalnzan la úvula.
• Grado 4: Amígdalas contactan en la línea media.
- Además, pruebas complementarias de imagen como puede ser la telerradiografía, ortopantomografía, scanner y resonancia magnética, nos ayudan a ver alteraciones morfológicas de la anatomía la cual puede tener relación con SAHS. En ningún momento estas pruebas son diagnóstico concluyente ya que de eso se encarga el médico especializado.
Debemos ser capaces de reconocer todos estos signos y síntomas porque en caso de que el paciente no esté diagnosticado del SAHS y sospechemos de elo será importante derivarlo al médico con el objetivo de realizar un diagnóstico definitivo y así luego poder realizarle un tratamiento. En nuestro ámbito utilizaremos aparatos intraorales que se adaptarán a la estructura oral de cada paciente, permitiendo avanzar la mandíbula unos milimetros para que la vía aérea aumente. A continuación hablaremos del tratamiento de la apnea del sueño que podemos realizar en una clínica odontológica. 4. TRATAMIENTO y NUEVOS MATERIALES:
Después del diagnóstico por parte del médico espealizado, el tratamiento que se utiliza es un tratamiento multifactorial en el cual nosotros como odontólogos podemos participar. Como ya hemos dicho anteriormente realizando aparatos intraorales.
El diagnóstico suele realizarse mediante la polisomnografía ya que es el medio de elección y el registro más completo para la certeza del diagnóstico. Resumidamente para no entrar en materia se trata de registrar la actividad cerebral, respiración, ritmo cardiaco, actividad muscular y también de los niveles de oxígeno mientras se duerme. Registra funciones corporales cuando uno duerme o empieza a dormir.
El tratamiento ya hemos dicho que tiene muchos factores.
- Primero hay que realizar unas medidas generales, estas son las siguientes:
• Higiene del sueño: hay que establecer un protocolo de sueño, es decir intentar un horario regular del ciclo sueño-vigilia.
• Control de peso: en el caso de que presente obesidad o sobrepeso, como ya hemos dicho que esto aumenta la obstrucción de la VAS, reducir el peso ayuda a mejorar las situaciones graves de la enfermedad. Modificar el estilo de vida y los habitos alimenticios es lo que se debe conseguir, aunque a veces es bastante complicado.
• Hábitos nocivos como el tabaco o el alcohol tienen que evitarse o al menos retringirse.
• Fármacos como benzodiacepinas, antihistamínicos, barbitúricos y opiáceos son depresores y sedantes del sistema nervioso central, debemos saber que favorecen la obstrucción de la VAS. Por eso también un paciente diagnosticado de SAHS que acude a la consulta odontólogica y es ansioso en situaciones de tratamientos dentales, deberemos acudir a otros fármacos.
-
- Tratamiento con presión positiva CPAP (Continuous positive air pressure). Es el tratamiento principal. Este tratamiento consiste en un dispositivo de una turbina que genera un flujo continuo de aire con una presión. El flujo continuo de aire puede ser programado y el nivel de presión se mantiene constante. También puede comenzarse con una presión baja y a medida aumenta para mejorar la conciliación del sueño. La máquina consta de un tubo que a su vez recibe en el otro extremo una mascarilla. Al aumentar la presión dentro de la VAS, evita la aparición de apneas o hipoapneas. 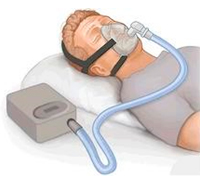 - El tratamiento quirúrgico o roncocirugía, tiene numerosos procedimientos dependiendo de lo que cause el SAHS, es decir, varía desde una traqueotomía hasta un adelantamiento del geniogloso, reducción de la base de la lengua, adenoidectomía en el caso de las amígdalas... todo aquello que favorezca la obstrucción de la VAS. En cuanto a la cirugía maxilofacial realizando un adelantamiento bimaxilar puede darse, pero es un tratamiento para pacientes con características esqueletales y estéticas determinadas.
- Tratamiento con aparatología intraoral. Según su mecanismo de acción los podemos dividir en cuatro tipos.
• Aparatología de reposicionamiento anterior de la lengua (TRD).
• Aparatología de reposicionamiento anterior de la mandíbula (MAD).
• Aparatología de elevación del velo del paladar y reposicionamiento de la úvula (ASPL).
• Aparatología de presión oral positiva (OPAP).
Actualmente los aparatos de avance mandibular son los más utilizados para el tratamiento del SAHS. Los posicionadores anteriores de la lengua y los destinados a la elevación del velo del paladar suelen estar ya en desuso.
• TRD: Actuan manteniendo la lengua en una posición más adelantada pero no avanza la mandíbula. Entonces aumena el espacio aéreo posterior. Mantiene la lengua en una posición adelantada por succión, ya que anteriormente se sitúa un bulbo acrílico que crea una presión negativa en su interior al introducir la lengua durante el sueño. Para pacientes edéntulos totales sería el dispositivo más adaptado. 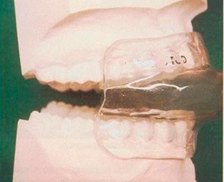 • MAD: Es el grupo más extenso de los dipositivos intraorales para el tratamiento del ronquido y SAHS. A diferencia de los anteriores, estos generan un avance de la mandíbula y aumenta el espacio aéreo.El avance mandibular también induce cambios en el hueso hioides, haciendo que este se situe en una posición más anterior o adelantada. La lengua se situa anteriormente y se realiza una tracción de la pared faringea anterior.
Todavía se puede manifestar que los aparatos intraorales y en preciso, los MAD, constituyen un tratamiento eficaz en estos pacientes. Aunque la respuesta no es la misma en todos los pacientes, las prótesis de avance mandibular estarían indicadas para tratar este tipo de trastorno.
Ya que este apartado de aparatos intraorales es muy amplio, haremos hincapié en alguno.
NAPA (Nocturnal Airway Patency Appliance®): Hay dos diseños.
Diseño original en el cual hay una protrusión mandibular de ¾ de la distancia entre oclusión céntrica y máxima protrusión mandibular. Se realizan avances mandibulares entre 6 y 9 milímetros (mm) de apertura anterior. Es un acrílico con 6-8 ganchos como sistema de anclaje y una prolongación acrílica hueca en su interior. 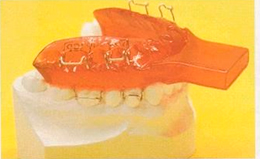 Figura 4.
El otro diseño fue perforado en las zonas laterales, con el propósito de facilitar el paso de aire. 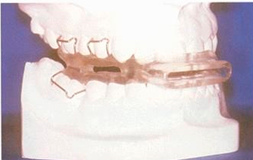 Herbst Se utiliza bastante por los odontólogos, sobre todo en clases II con retrognatismo mandibular. Se manipulan varias férulas de acrílico solidarizadas con dos bielas en acero que rigen la propulsión. Se incluyen algunas modificaciones como son: la figura de dos ganchos de bola en la férula superior entre canino y premolar, para poner dos elásticos intermaxilares, uno a cada lado, entre la férula superior e inferior. Su objetivo es mantener ambas arcadas en posición cerrada durante el sueño, para aumentar la retención de ambas férulas con ganchos de bola.
A veces, los pacientes presentan falta de piezas dentales y son portadores de prótesis removibles, a lo que otros autores modificaron el Herbst utilizando la prótesis superior esquelética como anclaje de las bielas. 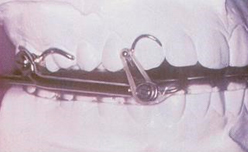 SAS de Zurich®. Es un aparato monobloque rígido que consta de dos placas de acrílico, superior e inferior. Se conectan por medio de alambres de forma rectangular doblado en W. De esta forma hay un espacio mayor para la lengua y facilita el flujo de aire. Además, se utiliza menos cantidad de acrílico. El aparato se fabrica con avance mandibular de 3/4 de la máxima protrusiva posible y una apertura vertical entre 8 y 12 mm. El anclaje del aparato se fortifica mediante ganchos entre los primeros premolares y primeros molares. La mandíbula está en una posición protruída y un poco abierta. 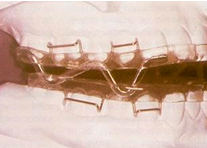 Posicionadores elásticos de avance mandibular. Conjunto de muchos dispositivos monobloque elásticos. Se suelen utilizar en ortodoncia y realizan un avance mandibular reversible como el reposicionamiento anterior de la lengua. También se utilizan para el SAHS. Para su fabricación se utiliza silicona blanda unidos por una mordida en cera y se monta en un articular semiajustable. 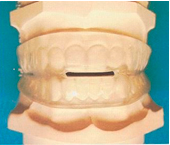 Aparatología de elevación del velo del paladar y reposicionamiento de la úvula. Estos aparatos ya casi están en desuso y consiste en elevar el velo del paladar y reposicionar la úvula hacia una posición más superior. Podemos distinguir varios aparatos, uno de ellos es el Equalizer (Equalizer Airway 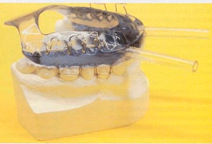 Figura 9.
Lo podemos considerar un aparato híbrido entre MAD y elevación del velo y reposicionamiento de la úvula ya que debido a la extensión posterior de acrílico eleva el velo del paladar y además provoca un avance mandibular. Presenta dos tubos plásticos situados en su parte anterior, con el fin de igualar la presión de aire intraoral y extraoral, sin dañar la respiración nasal. Pueden completarse con diferentes sistemas de anclaje para aumentar el grado de retención en la boca. Es útil para el tratamiento del SAHS.
• Aparatología OPAP. Dispositivo que consta de un MAD y un CPAP. 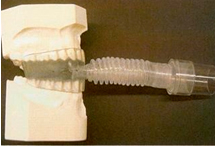 Figura 10.
Todos estos dispositivos tienen un objetivo común y es que disminuya la probabilidad de que haya una obstrucción de la VAS y desaparezca, si se puede, el ronquido. En la siguiente radiografía de cráneo tomada desde una proyección lateral (telerradiografía), podemos observar que la figura 11 está sin dispositivo intraoral y en la figura 12 sí que lo tiene, pudiendo ver como se ve aumentado el espacio aéreo en la zona posterior de la lengua. 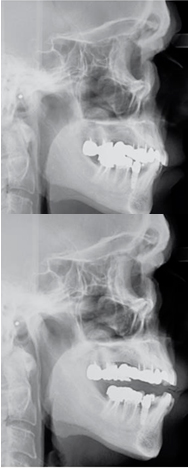
Figura 11. Proyección lateral del cráneo y estructuras maxilares donde el paciente está sin dispositivo intraoral.
Figura 12. Proyección lateral
del cráneo y estructuras maxilares donde el paciente está con dispositivo intraoral. Espacio aéreo posterior a la
lengua se ve aumentado. Debido a que hay un gran número de aparatos intraorales, deberemos escoger el más adecuado para al paciente. Está condicionado por varios factores como pueden ser la facilidad de uso, la capacidad de movimiento mandibular, la comodidad para el paciente y si hay alguna patología como el bruxismo. Ya que es una patología en la que aumenta el riesgo de romperse o de repercutir a nivel de la articulación temporomandibular o muscular.
Una vez elegido el más conveniente para el paciente, será necesario coger las medidas para la elaboración de los modelos de trabajo. Se realizarán dos impresiones, tanto de la arcada superior como de la arcada inferior. Hay que tener en cuenta que la opción del registro de mordida determinará la mandíbula una vez puesto el dispositivo. En algunos dispositivos necesitaremos un registro de cera de oclusión. En otros dispositivos, como pueden ser los de MAD, necesitaremos un registro en cera o silicona de la protrusión mandibular que necesitemos. Para ello necesitaremos instrumentos (instrumento de George) que nos permitan fijar la mandíbula en el máximo grado de protrusión del paciente y adaptarlo. De esa forma nos permite más fácilmente tomar el registro deseado, ya que está fijado. Después de realizar esto, los modelos y el registro de mordida se envían al laboratorio para que realicen los modelos.
También es conveniente realizar fotografías extraorales e intraorales del paciente.
5. PAUTAS PARA EL PACIENTE
Una vez que el paciente tenga el dispositivo, será esencial instruirlo para su cuidado.
En cuanto a higiene del dispositivo, le explicaremos que cada mañana después de su uso tendrá que limpiarse con un cepillo dental, agua tibia y un jabón antibacteriano. Enjuagar bien y secar antes de guardarlo. Se deberá desinfectar a menudo con pastillas para la limpieza de prótesis.
Además, deberemos recordar al paciente que pueden aparecer efectos secundarios como un malestar dental leve, exceso de saliva los primeros días, dolor en la mandíbula, movilidad dental o incluso dolor en la articulación temporomandibular. Estos efectos deberán ser comunicados al odontólogo por si fuera necesario la posterior confección de otro dispositivo o ajustar el mismo.
6. BIBLIOGRAFÍA 1. Bodenner KA, Jambhekar SK, Com G, . Assessment and treatment of obstructive sleep-disordered breathing. Clin Pediatr. 2014;53:544-548. 2. Maris M, Verhulst S, Wojciechowski M, . Prevalence of obstructive sleep apnea in children with Down syndrome. Sleep. 2016;39:699-704. 3. de Miguel-Diez J, Villa-Asensi JR, Alvarez-Sala JL. Prevalence of sleep-disordered breathing in children with Down syndrome: polygraphic findings in 108 children. Sleep. 2003;26:1006-1009. 4. Park JG, Ramar K, Olson EJ. Updates on definition, consequences, and management of obstructive sleep apnea. Mayo Clin Proc. 2011;86:549-555. 5. Lefaivre JF, Cohen SR, Burstein FD, . Down syndrome: identification and surgical management of obstructive sleep apnea. Plast Reconstr Surg. 1997;99:629-637. 6. Beebe DW, Gozal D. Obstructive sleep apnea and the prefrontal cortex: towards a comprehensive model linking nocturnal upper airway obstruction to daytime cognitive and behavioral deficits. J Sleep Res. 2002;11:1-16. 7. Berry RB, Budhiraja R, Gottlieb DJ, . Rules for scoring respiratory events in sleep: update of the 2007 AASM Manual for the Scoring of Sleep and Associated Events. Deliberations of the Sleep Apnea Definitions Task Force of the American Academy of Sleep Medicine. J Clin Sleep Med. 2012;8:597-619. 8. Mitchell RB, Kelly J. Outcome of adenotonsillectomy for obstructive sleep apnea in obese and normal-weight children. Otolaryngol Head Neck Surg. 2007;137:43-48. 9. Bhattacharjee R, Kheirandish-Gozal L, Spruyt K, . Adenotonsillectomy outcomes in treatment of obstructive sleep apnea in children: a multicenter retrospective study. Am J Respir Crit Care Med. 2010;182:676-683. 10. Merrell JA, Shott SR. OSAS in Down syndrome: T&A versus T&A plus lateral pharyngoplasty. Int J Pediatr Otorhinolaryngol. 2007;71:1197-1203.
11. Shete MM, Stocks RM, Sebelik ME, . Effects of adeno-tonsillectomy on polysomnography patterns in Down syndrome children with obstructive sleep apnea: a comparative study with children without Down syndrome. Int J Pediatr Otorhinolaryngol. 2010;74:241-244.
12. Thottam PJ, Trivedi S, Siegel B, . Comparative outcomes of severe obstructive sleep apnea in pediatric patients with trisomy 21. Int J Pediatr Otorhinolaryngol 2015;79:1013-1016. 13. Thottam PJ, Choi S, Simons JP, . Effect of adenotonsillectomy on central and obstructive sleep apnea in children with Down syndrome. Otolaryngol Head Neck Surg. 2015;153:644-648. 14. Slim K, Nini E, Forestier D, . Methodological index for non-randomized studies (minors): development and validation of a new instrument. ANZ J Surg. 2003;73:712-716. 15. Lewis S, Arjomandi H, Rosenfeld R. Systematic review of surgery for persistent pediatric tracheocutaneous fistula. Laryngoscope. 2017;127:241-246. 16. Maris M, Verhulst S, Wojciechowski M, . Outcome of adenotonsillectomy in children with Down syndrome and obstructive sleep apnoea [published online August 2, 2016]. Arch Dis Child. 17. Friedman M, Wilson M, Lin HC, . Updated systematic review of tonsillectomy and adenoidectomy for treatment of pediatric obstructive sleep apnea/hypopnea syndrome. Otolaryngol Head Neck Surg. 2009;140:800-808.
18. Harris N, Rosenberg A, Jangda S, . Prevalence of obesity in International Special Olympic athletes as determined by body mass index. J Am Diet Assoc. 2003;103:235-237
19. Bauer J, Teufel U, Doege C, . Energy expenditure in neonates with Down syndrome. J Pediatr. 2003;143:264-266. Google Scholar CrossRef, Medline
20. Costa DJ, Mitchell R. Adenotonsillectomy for obstructive sleep apnea in obese children: a meta-analysis. Otolaryngol Head Neck Surg. 2009;140:455-460. 21. Donnelly LF, Shott SR, LaRose CR, . Causes of persistent obstructive sleep apnea despite previous tonsillectomy and adenoidectomy in children with Down syndrome as depicted on static and dynamic cine MRI. Am J Roentgenol. 2004;183:175-181. 22. Fricke BL, Donnelly LF, Shott SR, . Comparison of lingual tonsil size as depicted on MR imaging between children with obstructive sleep apnea despite previous tonsillectomy and adenoidectomy and normal controls. Pediatr Radiol. 2006;36:518-523. 23. Sedaghat AR, Flax-Goldenberg RB, Gayler BW, . A case-control comparison of lingual tonsillar size in children with and without Down syndrome. Laryngoscope. 2012;122:1165-1169. 24. Brooks LJ, Olsen MN, Bacevice AM, . Relationship between sleep, sleep apnea, and neuropsychological function in children with Down syndrome. Sleep Breathing. 2015;19:197-204.
25. Kamm M, Burger R, Rimenzsberger P et al. Survey of children supported by long-term mechanical ventilation in Switzerland. Swiss Med Wkly 2001;131:261-6. [
26. Fauroux B, Boffa C, Desguerre I et al. Long-term noninvasive mechanical ventilation for children at home: a national survey. Pediatr Pulmonol 2003;35:119-25. 27. Edwards EA, Hsiao K, Nixon GM. Paediatric home ventilatory support: the Auckland experience. J Paediatr Child Health 2005;41:652-8. 28. Gowans M, Keenan HT, Bratton SL. The population prevalence of children receiving invasive home ventilation in Utah. Pediatr Pulmonol 2007;42:231-6. 29. Graham RJ, Fleegler EW, Robinson WM. Chronic ventilator need in the community: a 2005 pediatric census of Massachusetts. Pediatrics 2007;119:1280-87. 30. Racca F, Bonati M, Del Sorbo L et al. Invasive and non-invasive long-term mechanical ventilation in Italian children. Minerva Anestesiol 2011;77:892-901. 31. Wallis C, Paton JY, Beaton S et al. Children on long-term ventilatory support: 10 years of progress. Arch Dis Child 2011;96:998-1002. 32. Sovtic A, Minic P, Vukcevic M et al. Home mechanical ventilation in children is feasible in developing countries. Pediatr Int 2012;54:676-81. 33. González Cortés R, Bustinza Arriortua A, Pons Ódena M et al. Domiciliary mechanical ventilation in children: a Spanish multicentre study. An Pediatr (Barc) 2013;78:227-33. 34. McDougall CM, Adderley RJ, Wensley DF et al. Long-term ventilation in children: longitudinal trends and outcomes. Arch Dis Child 2013;98:660-5. 35. Amin R, Sayal P, Syed F et al. Pediatric long-term home mechanical ventilation: twenty years of follow-up from one Canadian center. Pediatr Pulmonol 2014;49:816-24. 36. Appierto L, Cori M, Bianchi R et al. Home care for chronic respiratory failure in children: 15 years experience. Paediatr Anaesth 2002;12:345-50. 37. Teague WG. Non-invasive positive pressure ventilation: current status in paediatric patients. Paediatr Respir Rev 2005;6:52-60. 38. Pavone M, Verrillo E, Caldarelli V et al. Non-invasive positive pressure ventilation in children. Early Hum Dev 2013;89(Suppl 3):S25-31. 39. Fauroux B, Louis B, Hart N et al. The effect of back-up rate during non-invasive ventilation in young patients with cystic fibrosis. Intensive Care Med 2004;30:673-81. 40. Fauroux B, Nicot F, Essouri S et al. Setting of noninvasive pressure support in young patients with cystic fibrosis. Eur Respir J 2004;24:624-30. 41. Fauroux B. Why, when and how to propose noninvasive ventilation in cystic fibrosis? Minerva Anestesiol 2011;77:1108-14. 42. Flight WG, Shaw J, Johnson S et al. Long-term non-invasive ventilation in cystic fibrosis-Experience over two decades. J Cyst Fibrosis 2012;11:187-92. 43. Guilleminault C, Philip P, Robinson A. Sleep and neuromuscular disease: bilevel positive airway pressure by nasal mask as a treatment for sleep disordered breathing in patients with neuromuscular disease. J Neurol Neurosurg Psychiatry 1998;65:225-32. 44. Baydur A, Layne E, Aral H et al. Long term non-invasive ventilation in the community for patients with musculoskeletal disorders: 46 year experience and review. Thorax 2000;55:4-11. 45. Mellies U, Dohna-Schwake C, Stehling F et al. Sleep disordered breathing in spinal muscular atrophy. Neuromuscular Disord 2004;14:797-803. 46. Suresh S, Wales P, Dakin C et al. Sleep-related breathing disorder in Duchenne muscular dystrophy: disease spectrum in the paediatric population. J Paediatr Child Health 2005;41:500-3. 47. Ward S, Chatwin M, Heather S et al. Randomised controlled trial of non-invasive ventilation (NIV) for nocturnal hypoventilation in neuromuscular and chest wall disease patients with daytime normocapnia. Thorax 2005;60:1019-24. 48. Simonds AK. Recent advances in respiratory care for neuromuscular disease. Chest 2006;130:1879-86.
|
 Información General
Información General Artículos
Artículos Notícias
Notícias Enlaces
Enlaces Contactar
Contactar Buscar
Buscar Premio Nadal
Premio Nadal Formación Continuada
Formación Continuada
